Biotechnology関連の研究
たんぱく質の反応場としてのイオン液体
たんぱく質・生体分子の新規溶媒としての水和イオン液体の提案
イオン液体中における酸化還元酵素の電極反応
非接触光導波路分光法の開発
たんぱく質の反応場としてのイオン液体
イオン液体はたんぱく質の反応溶媒としても注目されている。しかし、たんぱく質は、水以外の液体に対して不溶であり、溶解しても変性してしまう。そのため。基本的にはイオン液体に溶解できないと考えられている。しかし、極性高分子の一種であるポリエチレンオキシド(PEO)をたんぱく質に化学修飾することで、イオン液体に溶解することが可能になる。我々は電子伝達たんぱく質の一種であるウマ心筋由来シトクロムc (以下、cyt.c)にPEOを化学修飾することで、イオン液体中への可溶化を報告した(Chem. Lett., 2003, 32, 450. Link)。未修飾cyt.cは一般的なイオン液体である[C4mim][Tf2N]に溶解しないが、平均分子量2000のPEOを修飾すると溶解するようになる(Figure 1)。溶解したPEOを修飾したcyt.c(PEO-cyt.c)は水中に溶解しているcyt.cと同様に、408nmに最大吸収波長を有する吸収スペクトルを示した。[C4mim][Tf2mN]中に溶解しただけではPEO-cyt.cは酸化還元応答を示さないが、KClを加えることで酸化還元反応を示すことを明らかにした。
![(a)[C4mim][Tf2N]中に導入したcyt c (左)とPEO-cyt c (右)<br>(b) イオン液体中に溶解したPEO-cyt cの電極応答に基づくスペクトル変化](img/fig3-1-1.jpg)
Figure 1. (a)[C4mim][Tf2N]中に導入したcyt.c(左)とPEO-cyt.c(右)
(b) イオン液体中に溶解したPEO-cyt.cの電極応答に基づくスペクトル変化
また、PEOを修飾しなくてもイオン液体の極性をデザインにより制御することで、cyt.cを大きな構造変化を引き起こすことなく溶解できることを確認した(Biotechnol. Bioeng., 2012, 109, 729. Link)。イオン液体の極性値をKamlet-Taftパラメータを用いて算出したところ、水素結合受容性(β値)と双極性(π*値)がそれぞれ0.7、1.17以上のイオン液体がチトクロムcを高濃度に溶解可能であることが明らかとなった(図)。中でもポリエチレンオキシドと同様のエーテル酸素を導入した1-allyl-3-methylimidazolium ([amim])カチオンとクロライドアニオンからなる[amim]Cl中に溶解したcyt.cは活性中心の構造を保持したまま溶解し、140℃という高温下においても酸化還元応答が観測された(Figure 2)。イオン液体中にたんぱく質を溶解させることで、利用可能な温度域を大幅に拡大できるものと期待される。
![(a)[C4mim][Tf2N]中に導入したcyt c (左)とPEO-cyt c (右)<br>(b) イオン液体中に溶解したPEO-cyt cの電極応答に基づくスペクトル変化](img/fig3-1-2.jpg)
Figure 2. (左)イオン液体のKamlet-Taftパラメータとcyt cの溶解性の相関,
(右)[amim]Cl中に溶解したcyt.cの140℃および80℃下の電極応答に基づくスペクトル変化
たんぱく質・生体分子の新規溶媒としての水和イオン液体の提案
一般的なイオン液体中へのタンパク質の溶解は難しいが、タンパク質への化学修飾や、イオン液体の構造デザインにより溶解が可能となることを前項で示した。ここでは、化学修飾などを必要とせず、様々なタンパク質をイオン液体中に溶解可能な"水和イオン液体"を紹介する。水和イオン液体は、イオン液体にわずかな量の水を添加して作成する。水和イオン液体中に存在する水は水和状態であり、バルク中の自由水とは異なる。イオン構造を選択した水和イオン液体を用いることで、様々な種類のタンパク質や、核酸など生体分子がbuffer中と同様の高次構造を保持したまま溶解可能であることを報告してきた(Biopolymers, 2010, 93, 1093. Link, Chem. Commun., 2012, 48, 5751. Link)。水和イオン液体を溶媒としてタンパク質を溶解することで、タンパク質の耐熱性や経時安定性が水溶液中に比べて格段に向上することを明らかにした。タンパク質によっては、熱変性温度がbuffer中に比べて20度以上上がり、さらに常温で1年半以上保存後も高い活性を保持していることを報告している(Biomacromolecules, 2007, 8, 2080. Link)。
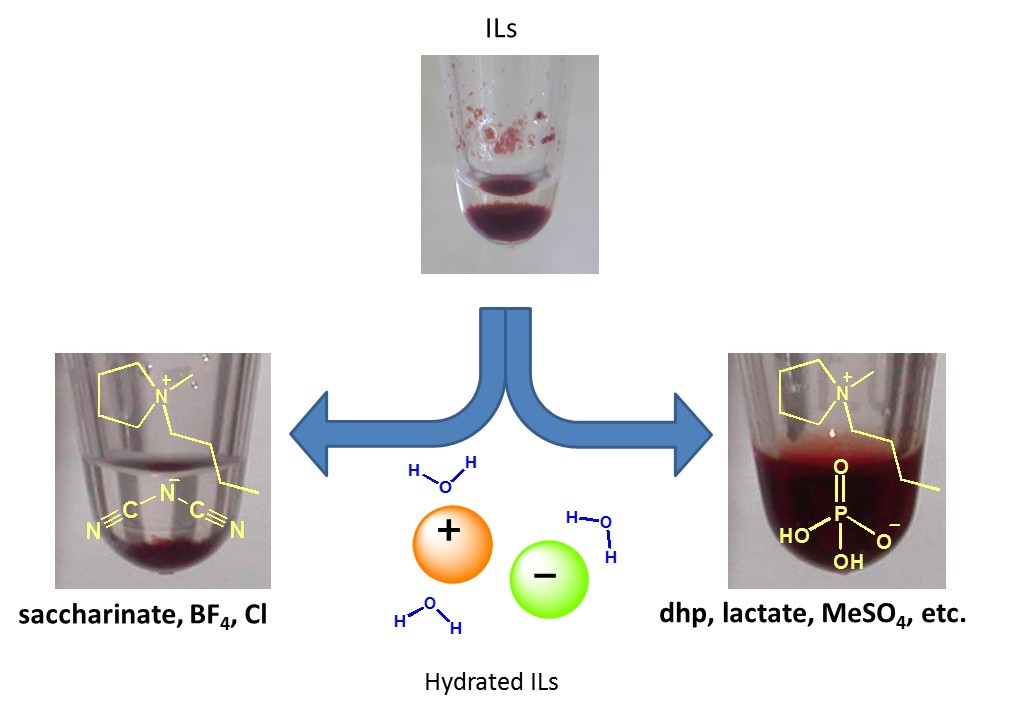
Figure 3. 水和イオン液体を用いたタンパク質の溶解性の違い
また、水和イオン液体中に溶解したタンパク質は、含水率を調整することで水和イオン液体中でも酵素反応(Green Chem., 2009, 11, 351. Link)や電子移動反応が進行することも報告した。(水和イオン液体中で電子移動反応についての詳細は次項に示した。)さらに、水和イオン液体中への溶解によるタンパク質のリフォールディング効果が示唆されており、現在検討中である。
水和イオン液体をタンパク質や生体分子の溶媒とすることで、興味深い結果が得られているが、構成するイオンや水の添加量によってタンパク質への影響は大きく異なる。我々は現在のところ、イオンの水の形成能を示すコスモトロピシティがタンパク質の溶媒としての水和イオン液体の性質に関与しているのではないかと考えている。希薄な水溶液中において、タンパク質の活性等にコスモトロピシティが関与することは以前より報告されてきたが、類似する効果が水和イオン液体中でもあると予測される。コスモトロピシティの異なるイオン種から構成される水和イオン液体を用いて解析を行った結果、同じモル比で存在している水でも性質が大きく異なることが明らかとなった。特に、DSC測定を用いて行った検討では、水の低温での結晶化(コールドクリスタリゼーション)を示す水和イオン液体が存在することが分かった。詳細は割愛するが、このコールドクリスタリゼーションを示すような水和イオン液体中では、タンパク質が溶解し、さらに高次構造を保持する可能性が高いことが示された(Chem. Commun., 2013, 49, 3257. Link)。イオン液体を用いることで、存在する水分子のモル数や量を規定することが可能であり、これまで希薄系では観測できなかった水とタンパク質、生体分子との相間についての詳細な解析が期待できる。今後もイオンと水がタンパク質に及ぼす影響について検討をすすめていく予定である。
イオン液体中における酸化還元酵素の電極反応
バイオ燃料電池は、生体由来の物質(微生物もしくは酵素)を触媒として用いて、糖やアルコールといった燃料から電気エネルギーを取り出すデバイスである。生体由来の触媒を用いるため、温和(室温、中性)な条件下で作動するという利点があり、次世代のエネルギーデバイスとして有望である。酵素などの生体物質を用いる場合、溶媒は一般的に水であり、これまでのバイオ燃料電池の研究でも溶媒には水が用いられてきた。しかしながら、溶媒として水を用いることによって生じるデメリットも多い。例えば、使用温度域は水が液体である0-100 ℃に制限される上、水の揮発や生体物質の腐敗に起因してデバイスの長期安定性が低いことなどがあげられる。イオン液体をバイオ燃料電池の溶媒として利用できれば、これらの課題を解決し、極限環境にも耐えうるバイオ燃料電池の作製が可能になると考えられる。これに加え、水に溶けにくい物質を燃料として利用できる可能性もある。イオン液体中での酸化還元酵素の電極反応について調べることは、イオン液体を電解質として用いた酵素バイオ燃料電池を作製するために重要なステップである。イオン液体中における酸化還元酵素の電極反応を実現するには、適切なイオン液体を選択すること、酸化還元酵素の電極への固定化を工夫することなどが求められる。ここでは、イオン液体中における酸化還元酵素の電極反応に関する研究を紹介する。
水和[ch][dhp]がタンパク質の保存溶媒、反応場として優れた性質をもつことを前項ですでに述べた。バイオ燃料電池のアノードで検討されている酵素電極について、水和[ch][dhp]中で電気化学的解析を行った。ナノ粒子を修飾した電極上にフルクトース脱水素酵素を固定化して、水和[ch][dhp]中での電極応答を観察した(Electrochim. Acta, 2011, 56, 7224. Link)。フルクトースが存在しない場合には電流値は観測されなかったのに対して、フルクトースの添加により触媒電流が流れることが認められた(Figure 4)。同様に、セロビオース脱水素酵素も電極との電子伝達が可能であり、電極表面に固定されたセロビオース脱水素酵素は3週間後も電極応答を示した。従来用いられてきた緩衝液(水)中よりも長期間にわたって電気化学的な活性を維持しており、水和[ch][dhp]がバイオ燃料電池の耐久性向上に寄与することを強く期待させる結果である。
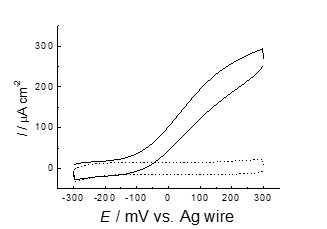
Figure 4. フルクトース脱水素酵素を固定化した電極のサイクリックボルタモグラム
(実線:フルクトースあり、点線:フルクトースなし)
カソード触媒として一般的に利用されるビリルビン酸化酵素(BOD)についても、イオン液体中での電極反応を検討している。BODは酸素の4電子還元反応を触媒するマルチ銅酸化酵素である。金ナノ粒子を修飾した電極をBOD水溶液に浸漬して、酵素電極を作製した。この電極を用いて種々のイオン液体中で電気化学的解析を行ったところ、親水性のイオン液体中では酸素の還元電流は観測されなかった。しかしながら、疎水性のbis(trifluoromethanesulfonyl)imide ([Tf2N])アニオンをもちつつ、カチオンに極性基を導入した1-(2-hydroxyethyl)-3-methylimidazolium bis(trifluoromethanesulfonyl)imide ([C2OHmin][Tf2N])にごく少量の水を添加すると良好な触媒電流が得られた(Catalysis Today, 2013, 200, 49. Link)。解析の結果、イオン液体中の水の状態が触媒電流値に大きく影響することをつきとめた。さらには、この電極を用いて、イオン液体を電解質とする酵素バイオ燃料電池を世界で初めて報告した(Biosensors and Bioelectronics, 2013, 39, 334. Link)。電池特性には改善の余地があるものの、これらの研究を皮切りにして、紙などを投入するだけで発電できるワンポット発電システムが実現する未来もそう遠くないかもしれない。
非接触光導波路分光法の開発
界面はバルクとは異なる性質を持ち、バルクでは観測されないような分子挙動や反応が生じることから、様々な分野で界面解析が求められている。このような界面解析を行うため、様々な手法を用いた研究が進められていますが、困難な点が数多く存在する。
我々は、界面の解析方法として光導波路分光法を用いている。光導波路分光法は薄い導波路中に光を全反射させながら伝搬させ、反射する度に導波路からしみ出すエバネッセント波を用いて吸収スペクトルを得るという測定法である。さらに、我々はこのエバネッセント波のしみ込みに着目した非接触セルシステムを開発した(Figure 5) (Chem. Lett., 2000, 29, 76. Link)。このセルシステムは、エバネッセント波のしみ込む距離以内に測定基板を固定することで、非接触で基板界面の測定が可能となる。このセルシステムを用いることで、これまで不可能だった金電極や炭素電極など透光性のない電極上に存在する分子の吸収スペクトル解析が可能となった。基本的には、あらゆる基板上の解析が可能となる。
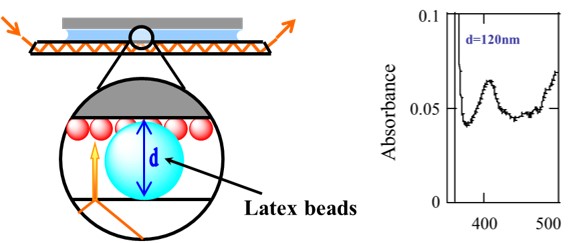
Figure 5. 非接触光同派路分光法の模式図(左)、電極上にチトクロムcが吸着した基板の非接触スペクトル(右)
この非接触光導波路分光法を用いて、規則的に作製されたLB膜中に存在する色素分子の状態や(Polym. Adv. Technol., 2004, 15, 567. Link)、電極に吸着したたんぱく質の電気化学的な挙動(Electrochem. Commun., 2003, 5, 47. Link)、さらに水中だけでなくPEO中やイオン液体中でのPEO修飾たんぱく質の挙動などについての解析(Polym. Adv. Technol., 2003, 14, 486. Link, Chem. Lett., 2003, 32, 450. Link)を行っている。

