Division of Applied Chemistry, Institute of Engineering, Tokyo University of Agriculture and Technology
研究内容Research
効率的で環境にやさしい複素環合成法の開発を目指しています。
複素環化合物は、医・農薬や機能性材料などの多くの有用物質に含まれる重要な化学物質です。しかしながら、汎用されている複素環合成法の多くは1)過酷な反応条件、2)多段階の合成反応、3)化学量論量以上の試薬などを必要とします。環境に調和した合成反応を重要視されている現代社会において、有用な複素環化合物を効率良く供給していく上で、新規かつ効率的な複素環合成法の開発は重要な課題です。
一方、触媒的連続反応は、1つのフラスコ内で単一の触媒系(ごく微量の活性化剤)が複数の反応を連続的に活性化するので、合成経路の短工程化・後処理の簡略化に寄与するだけでなく、化学排出物の軽減にも繋がります。このような観点から、効率的な複素環合成法の開発を指向して、金属触媒反応やメタルフリーな方法を用いた連続的な結合形成反応や多成分連結型反応に関する研究に取り組んでいます。
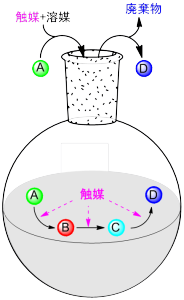
以下の複素環合成法は、最近開発した反応の一部です。
遷移金属触媒を用いる複素環合成法
a)アミノクライゼン転位型反応を基盤とするインドール合成法:N-プロパルギルアニリン誘導体は、金属触媒を用いると、一般的に環化反応が進行し、ジヒドロキノリン化合物を与えます。これに対して、我々が開発したRh(I)触媒系を用いると、アミノクライゼン転位型反応と中間体の環化反応が進行し、インドール化合物を与えます。
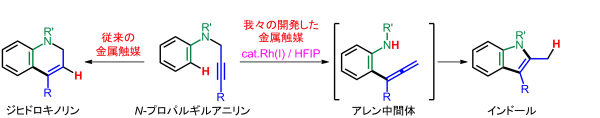
b)側鎖導入型オキサゾール合成法:プロパルギルアミド誘導体の環化異性化反応はオキサゾール化合物の簡便な合成法の一つです。我々は、プロパルギルアミド誘導体をPd(0)触媒存在下、アリル炭酸エステルと反応させると、オキサゾール骨格の構築と同時に側鎖にアリル基を導入できることを見出しました。
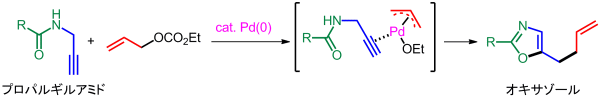
メタルフリーな複素環合成法
c) ヘテロ-エンインメタセシス反応を基盤とする三成分連結型イミノキノリン合成法:我々は、o-アルキニルアニリン誘導体とイミンとのヘテロ-エンインメタセシス反応を経由するイミノキノリン合成法を見出しました。本反応は、ヘキサフルオロイソプロパノール(HFIP)を溶媒とすることにより、無触媒で進行します。また、イミンの代わりに、アミンとアルデヒドを用いた3成分連結型の合成法にも適用可能です。
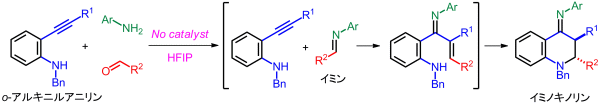
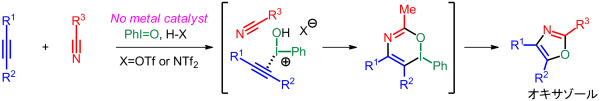
d) 超原子価ヨウ素試薬を用いる[2+2+1]型オキサゾール合成法:超原子価ヨウ素試薬は低毒性な酸化剤であり、ヨウ素原子の持つ金属と類似した反応は注目されています。我々は、アルキンとニトリルと超原子価ヨウ素試薬の酸素が1段階で連結する[2+2+1]型オキサゾール合成法を開発しました。このような合成法は従来、金属触媒を必要としていることから、従来法よりも環境にやさしい合成法となっています。
東京農工大学工学部応用分子化学科 齊藤研究室
〒184-8588
東京都小金井市中町2-24-16
TEL&Fax: 042-388-7667
E-mail: akio-sai@cc.tuat.ac.jp