丂愼怓懱(chromosome)偼妀傪峔惉偡傞庡側梫慺偱偁傝丄orcein, haematoxylin丆carmine側偳偺墫婎惈怓慺偵傛偔愼傑傞丅惷巭妀偱偼晛捠傒傞偙偲偼偱偒側偄偑丄暘楐傪奐巒偡傞偲巔傪偁傜傢偡丅桳巺暘楐(mitosis) 偼晛捠丄惷巭婜(resting stage乯丆慜婜乮prohase), 拞婜(metaphase),丂屻婜(anaphase)媦傃廔婜(trophase)偵暘偗傜傟傞偑丄愼怓懱偺娤嶡偵嵟傕搒崌偺傛偄偺偑拞婜偱偁傞丅
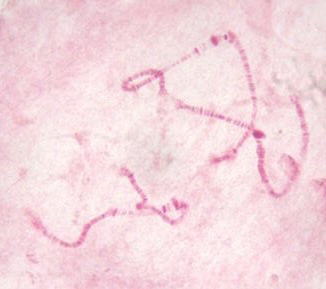 |
愼怓懱偲尵偊偽丄晛捠丄偙偺傛偆側巺忬偺傕偺傪憐憸偟傑偡丅 嵍恾偼儐僗儕僇偺懥塼態偺愼怓懱丅 |
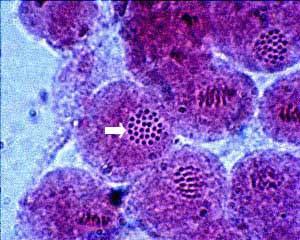 |
偟偐偟丄僇僀僐側偳偺椮憷栚偺愼怓懱偼仠忬乮敀栴報乯傪偟偰偄傑偡丅 戝偒偝丄挿偝側偳偱幆暿偡傞偺偼崲擄偱偡丅 壗屘丄娵偔側傞偺偐偼暘偐偭偰偄傑偣傫丅 嵍恾偼僇僀僐偺惛憙墴偟偮傇偟昗杮 |
丂
悈張棟墴偟偮傇偟朄
嵽椏丗俆椷俀擔栚偺亯梒拵乮偙偺帪婜偺惛憙偱偼拞婜偺妀偑嵟傕懡偔丄娤嶡偵揔偟偰偄傞乯丅
丂丂丂
1乯惛憙傪揈弌偡傞丅
丂丂惛憙丟暊晹戞俆娐愡丄惎忬栦偺壓偵偁傝丄惎忬栦偵儊僗傪偄傟傞偲娙扨偵旘傃弌偟偰偔傞丅
丂丂姷傟側偄偆偪偼梒拵傪暊懁偐傜夝朥偟偰扵偡丅
2乯忲棴悈拞偵20乣30暘娫曻抲偡傞乮嵶朎偑悈傪媧廂偟偰朿傟傞乯丅
3乯偙傟傪僗儔僀僪僌儔僗忋偵庢傝弌偟丄惛憙旐枌傪攋偭偰撪梕暔傪僗儔僀僪僌儔僗忋偵弌偡丅
4乯恷巁 orcein傪侾揌棊偲偟丄偦偺傑傑20暘娫曻抲偡傞丅
5乯僇僶亅僌儔僗傪偐偗偰寉偔墴偟偮傇偟偰尠旝嬀娤嶡傪峴偆丅
* 恷巁orcein ; 45%恷巁 100ml偵1g偺orcein傪梟偐偡丅
 |
掅攞棪偱偼嵍恾偺傛偆偵嵶朎幙偑敄偄愒丄妀傗愼怓懱偑擹偄愒偵愼傑偭偰尒偊傑偡丅 |
| 惛憙偺墴偟偮傇偟昗杮 | |
僇僀僐泱巕嵶朎偺愼怓懱偺娤嶡朄
| 帋栻 | |||
| 儕儞僈亅塼 | 0.85% NaCl悈梟塼 | 9.5ml | 僐儖僸僠儞偼掅擹搙偱戝偒側岠壥傪帵偡偑丄悈偵梟偐偟偨僐儖僸僠儞偼梋傝挿帩偪偟側偄丅1%塼偼嶌偭偰偐傜丄椻強偵曐懚偟偰栺1儢寧偼帩偨側偄丅彮検傪偙傑傔偵嶌偭偨曽偑妋幚偩偲巚偆丅 |
| 1%丂僐儖僸僠儞悈梟塼 | 0.5ml | ||
| 掅挘塼 | 1%丂僋僄儞巁僫僩儕僂儉 | 9.5ml | |
| 1%丂僐儖僸僠儞悈梟塼 | 0.5ml | ||
| 屌掕塼 | 儊僠儖傾儖僐亅儖 | 60ml | 屌掕塼偼巊梡捈慜偵嶌傞帠丅嶌傝抲偒偼晄壜丅 |
| 恷巁 | 20ml | ||
| 愼怓塼 | 僊儉僓尨塼 | 2.5m倢 |
娚徴塼偲僊儉僓尨塼傪崿偤偨嵺偵丄塼柺偵桘枌偑偱偒傞偑丄愼怓偺傓傜偵側傞偺偱鄅巻側偳偱庢傝彍偔丅 僊儉僓塼偺擹搙偼偦傟掱尩枾偱側偔偲傕傛偄丅2-8%埵偱愼怓帪娫丄悈愻帪娫偱愼怓擹搙傪挷愡偡傞丅 |
| pH6.8 偺1/15M 僛亅儗儞僙儞丒儕儞巁娚徴塼 | 50ml | ||
嵽椏
丂25亷嵜惵 3-4擔栚偺棏傪梡偄傞丅泱巕偼 stage17乮暊巿撍婲敪尰婜乯偐傜 stage21乮斀揮慜婜乯埲慜偺泱巕偑椙偄丅偦傟埲慜偺泱巕偱傕娤嶡偱偒傞偑丄泱巕偑惼偄偨傔偵庢傝弌偟偨傝丄僾儗僷儔亅僩嶌惉偵傗傗庤娫庢傞丅斀揮埲崀偺泱巕偱偼暘楐憸偑嬌傔偰彮側偔側傝丄傑偨旂晢偑岤偔側傞偨傔埖偄偵偔偄丅
曽朄
踢谑咦澳偺嶌惢
侾乯儕儞僈亅塼偺拞偱棏妅傪彍偒丄栺25亷偺僐儖僸僠儞擖傝偺儕儞僈亅塼偺拞偱栺3帪娫曻抲偡傞丅暘楐傪惙傫偵峴偭偰偄傞泱巕偱偁傟偽丄抁帪娫偱傕椙偄丅敪堢偺抶偄泱巕偱偼傗傗挿傔偵丄6帪娫埵曻抲偟偰傕摿偵塭嬁偼側偄偑丄12帪娫埲忋曻抲偡傞偲暘楐憸偑嬌傔偰懡偔側傝丄椬偺嵶朎偲嬫暿偑偟偵偔偔側傞丄傑偨丄惓忢側暘楐憸偑尭傝丄愼怓懱憸偺娤嶡偵偼揔偝側偔側傞丅
2乯僐儖僸僠儞擖傝儕儞僈亅塼拞偱燋塼枌傪攋傝丄泱巕傪庢弌偡丅
3乯泱巕傪掅挘塼偵堏偟丄梋暘偺塼偛偲僗儔僀僪丒僈儔僗偵堏偡丅
4乯10乣20暘幒壏偵曻抲偡傞丅偙偺娫偵傕僐儖僸僠儞偺岠壥偑偁傞偺偱曻抲帪娫偑抁偄偲巚傢傟傞応崌丄挿傔偵偡傞丅曻抲帪娫偑挿偄偲巚傢傟傞応崌偵偼抁偔偡傞丅
5乯梋暘側塼傪彍偒丄傗傗姡偐偡丅泱巕傪恓偱偽傜偽傜偵偡傞丅
6乯屌掕塼傪擖傟偨愼怓時偺忋偵抲偒丄屌掕塼偺婥壔僈僗偵栺侾暘偝傜偡丅偙偺張棟偵傛傝梋暘側塼傪泱巕偐傜彍偔帠偑偱偒丄巆偭偨塼傕屌掕塼偵撻愼傓丅僗儔僀僪丒僈儔僗傪愼怓時偵捑傔傞丅偙偺嵺丄泱巕偑姡憞偟偡偓偰偄傞偲愼怓懱偼娤嶡偟偵偔偄丅傑偨丄塼偑巆傝偡偓偰偄傞偲屌掕偑偆傑偔偄偐側偄丅
丂愼怓時拞偱10暘埲忋屌掕傪峴偆丅僗儔僀僪丒僈儔僗傪愼怓時偐傜庢弌偟丄鄅巻偺忋偵棫偰妡偗屌掕塼傪媧庢傞丅屌掕塼偑姡偒偒傞慜偵悈暯偵抲偒丄屌掕塼俙傪侾揌丄偝傜偵俁揌掱揌壓偡傞丅僗儔僀僪丒僈儔僗偺抂偵棴偭偨屌掕塼傪鄅巻偱媧庢傝丄1斢姡憞偝偣傞丅
俆乯埲壓偵偮偄偰偼師偺傛偆偵傕偱偒傞丅
丂梋暘側塼傪彍偒丄傗傗姡偐偡丅泱巕傪恓偱偽傜偽傜偵偡傞丅丄偙偺嵺丄泱巕偑姡憞偟偡偓偰偄傞偲愼怓懱偼娤嶡偟偵偔偄丅傑偨丄塼偑巆傝偡偓偰偄傞偲屌掕偑偆傑偔偄偐側偄
6乯屌掕塼傪1揌丄偝傜偵1揌揌壓偟丄屌掕塼偑僗儔僀僪丒僈儔僗偵峀偑傞偺傪懸偮丅僗儔僀僪丒僈儔僗偺抂偵梋暘側塼偑廤傑偭偰偔傞丅偙傟傪鄅巻摍偱媧偄庢傞丅姰慡偵姡偔慜偵屌掕塼傪偝傜偵2揌傎偳揌壓偡傞丅偙偺揌壓偺僞僀儈儞僌偼崱堜乮堚揱p101 I.-Q)傪嶲峫偵偡傞偲傛偄丅愭掱偲摨條偵僗儔僀僪丒僈儔僗偺抂偵梋暘側塼偑廤傑偭偰偔傞丅偙傟傪鄅巻摍偱媧偄庢傞丅1斢姡憞偝偣傞丅
愼怓
1乯愼怓塼傪擖傟偨愼怓時偵僗儔僀僪丒僈儔僗傪擖傟丄栺1帪娫愼怓偡傞丅
2乯愼怓屻丄悢昩悈愻偡傞丅僊儉僓偼悈偵梟偗傗偡偄偺偱拲堄偡傞丅
3乯阶材薅拮絺獖絺鐚皵鲖緜艎蠋@偱偒傞丅
幨恀傪庢傝偨偄応崌
1乯偝傜偵阶材薅拮絺饖畱S偵姡憞偝偣偨屻丄僉僔儗儞拞偵栺10暘擖傟丄扙悈偡傞丅
2乯僉僔儗儞偐傜庢傝弌偟丄僇僫僟僶儖僒儉側偳偺晻擖嵻傪侾丆俀揌揌壓偟丄僇僶乕掇捉傪偐偗晻擖偡傞丅
3乯悢擔屻丄僇僫僟僶儖僒儉偑屌傑偭偨傜尠旝嬀偱娤嶡偟丄幨恀傪嶣傞丅
憖嶌偺夋憸
嶨姶
仭掅挘塼偼嵶朎傪朿傜傑偣傞岠壥偑偁傞偲偄偆偑丄偁傑傝尠挊側岠壥偼柍偄傛偆偱偁傞丅
仭泱巕傪偽傜偽傜偵偡傞偺偵僩儕僾僔儞傗挻壒攇傪梡偄偨偑岠壥偼梋傝柍偐偭偨丅
丂屌掕塼偱偄偭偨傫屌掕偟偨屻偵 60%屌掕塼傪揌壓偟丄偦偺屻偵泱巕傪偽傜偽傜偵偡傞曽朄偱偼丄鉟楉側暘楐憸偑摼傜傟傞偑丄泱巕傪偽傜偽傜偵偡傞偺偑擄偟偔丄100敪100拞偲偄偆傢偗偵偼偄偐側偄傛偆偱偁傞丅
仭恷巁偑嫮偄応崌丄愒偔愼怓偝傟傞傛偆偱偁傞丅擕巁擖傝偺屌掕塼傪巊偆偲擹偔愼傑傞偲偄偆偑丄泱巕偱偼梋傝岠壥偼柍偄傛偆偱偁傞丅
仭pH6.8 偺1/15M 僛亅儗儞僙儞丒儕儞巁娚徴塼偺傛傝傕倫H10.0埵偺傾儖僇儕惈偺娚徴塼偺曽偑擹偔偦傑傞傛偆偩丅
丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂丂
栠傞